-
PROIZVODI
- Laboratorijski instrumenti
-
Laboratorijska oprema i opskrba
Opći potrošni materijal laboratorija InstrumentiUređaj
- Cijevi
- Dispenzeri i Droperi
- Grab Uzorkivači
- Kleme, Prstenovi i Stalci
- Ostale Aparature
- Pipete
- Pomagala za Pipete
- Posudice
- Posudice i Zdjelice
- Pribor za Vaganje
- Stalci
- Četke
- Štapići za Miješanje
Stakleno/plastično posuđe - Automatizirani laboratorijski sustavi
- Kemija, reagensi i standardi
- Mikrobiologija
- Laboratorijski mjerači i sonde
-
Online analizatori
EZ Series Analysers
- Iron
- Aluminium
- Manganese
- Phosphate
- Chloride
- Cyanide
- Fluoride
- Sulphate
- Sulphide
- Arsenic
- Chromium
- Copper
- Nickel
- Zinc
- Ammonium
- Total Nitrogen
- Total Phosphorus
- Phenol
- Volatile Fatty Acids
- Alkalinity
- ATP
- Hardness
- Toxicity
- Sample Preconditioning
- Boron
- Colour
- Nitrate
- Nitrite
- Silica
- Hydrogen Peroxide
- EZ Series Reagents
- EZ Series Accessories
- EZ sc Series Additional Analyzers
- EZ sc Series Inorganics
- EZ sc Series Metals
- EZ sc Series Nutrients
- Online senzori i kontroleri
- Claros Water Intelligence System
- Testni kompleti i trake
- Uzorkovanje
- Electrochemistry
- PARAMETRI
-
Softverska rješenja
-
Claros Sustav za inteligentno upravljanje vodom
Proizvodni stupovi Process Management
- Namjena rješenja:
- Otklanjanje BPK (BOD)/KPK (COD)
- Nitrifikacija/denitrifikacija
- Uklanjanje fosfora
- Upravljanje muljem
Data Management- Namjena rješenja:
- Prikupljanje
- Vizualizacija i analitika
- Izvještavanje
- Točnost podataka
Instrument Management- Namjena rješenja:
- Održavanje
- Rješavanje problema
- Udaljeni pristup
- Usporedba vrijednosti iz laboratorija i postupka
-
Claros Sustav za inteligentno upravljanje vodom
- Industrija
- PODRŠKA
- NOVOSTI I DOGAĐAJI
Croatia
Odaberite svoju zemlju ili regiju:
Europe
Americas
Asia - Australasia
- Australia
- Mainland China
- India
- Indonesia
- Japan
- Malaysia
- New Zealand
- Philippines
- Singapore
- South Korea
- Thailand (Thai)
- Taiwan
- Vietnam
Middle East - Africa
Karijere 042 305 086
Fosfor
Što je fosfor?
Fosfor (P) je kemijski element atomskog broja 15 i atomske mase 31. Zbog svoje visoke reaktivnosti fosfor prirodno ne postoji kao slobodni element. Fosfor se uglavnom pojavljuje kao fosfat u mineralima. Fosfat se obično nalazi u Zemljinoj kori u koncentraciji od oko 1 grama po kilogramu.
Dvije vrste elementarnog fosfora su bijeli i crveni fosfor. Kada se izloži kisiku, oksidacija dovodi do svjetlucanja bijelog fosfora (također poznato kao kemiluminiscencija).
Fosfor pripada dušikovoj skupini koja se sastoji od dušika, fosfora, arsena, antimona, bizmuta i ununpentija (od nedavno se naziva moskovij). Ti su elementi grupirani zbog slične atomske strukture, koja im daje sposobnost stvaranja stabilnih spojeva zbog njihove sklonosti stvaranju dvostrukih i trostrukih kovalentnih veza. Osim dušika (koji ostaje plin), ostali elementi iz dušikove skupine su krutine na sobnoj temperaturi.
Složenim organizmima poput biljaka i životinja potreban je fosfor jer su fosfati komponenta DNK, RNK, ATP i fosfolipida. Fosfor se vadi iz rudnika za uporabu u deterdžentima, pesticidima, nervnim agensima i pretežno gnojivima.
Fosfati/ortofosfat
U ortofosfatu (jednom od najčešćih fosfata) jedan je atom fosfora vezan za četiri atoma kisika. Ortofosfat se ponekad naziva i „reaktivni fosfor” jer se lako veže s drugim elementima i spojevima s manjkom elektrona, a tri „dodatna” elektrona na atomima kisika jako se žele vezati s protonima.
Kondenzirani fosfati
Kondenzirane fosfate čine više „kondenziranih” molekula ortofosfata koje dijele kovalentnu vezu između susjednih atoma fosfora (P) i kisika (O). Ova skupina uključuje metafosfat, pirofosfat i polifosfat – koji se često koriste za kontrolu korozije u vodoopskrbnim sustavima pitke vode.
Ukupni fosfor / organski fosfor
Ukupni fosfor zbroj je svih prisutnih fosfora: ortofosfata/fosfata, kondenziranih fosfata i organskog fosfora. Organski fosfor obično je prisutan u obliku fosfata sadržanih u organskom spoju ili vezanih s njime.
Zašto mjeriti fosfor?
Iako fosfati ne doprinose problemima s okusom i mirisom i stoga možda nisu bitni u vodi za piće, visoke razine fosfata u otpadnim vodama mogu značajno utjecati na okolni ekosustav. Visoka razina fosfata u izvornoj vodi može ubrzati rast algi i rast biljaka, što može dovesti do eutrofikacije i cvjetanja algi. Kada se to dogodi, ribama i vodenim organizmima uskraćuje se kisik, što rezultira velikim pomorom ribe i uništavanjem staništa. Mjerenje fosfata u otpadnim vodama od ključne je važnosti za održavanje zdravog ekosustava i zaštitu divljih životinja. Mnoga područja imaju stroga ograničenja za ispuštanje fosfata kako bi se zaštitio ekosustav u koji se ova voda ispušta. Osim zaštite ekosustava, ako se razine fosfata ne prate i ne kontroliraju, to može dovesti i do prekršaja i novčanih kazni. Pogoni za vodu za piće koji koriste fosfate za kontrolu korozije možda će trebati pratiti fosfate u finalnoj vodi, vodoopskrbnom sustavu i drugim fazama postupka obrade. Rješenja tvrtke Hach® stvorena su za održavanje sukladnosti i pružanje potrebnog znanja vašim operaterima za donošenje odluka o obradi.
Tvrtka Hach nudi potrebnu opremu za ispitivanje, resurse, obuku i softver kako biste uspješno pratili razine fosfora te njima upravljali na način specifičan za vaš radni postupak.
Istaknuti proizvodi za mjerenje fosfora
EZ Series Total Phosphorus Analyzers
Mrežni analizatori serije EZ nude višestruke mogućnosti za praćenje ukupnog fosfora u vodi.
Kupi sadaMrežni analizatori serije EZ nude višestruke mogućnosti za praćenje fosfora u vodi.
Kupi sadaHach je inovator u spektrofotometriji i nudi mnoge vodeće spektrofotometrijske instrumente na tržištu analize vode.
Kupi sadaBilo da tražite jedan uređaj za ispitivanje parametara kao što je DR300 ili napredniji instrument poput DR900 koji može mjeriti mnoge parametre s do 90 metoda, imamo rješenje za vas.
Kupi sada
Koji postupci zahtijevaju praćenje fosfora?
Voda za piće
Izvorna voda može sadržavati povišene koncentracije fosfata zbog poljoprivrednog otjecanja, što može uzrokovati eutrofikaciju površinskih voda rastom algi i oslobađanjem cijanotoksina. Kondenzirani fosfati često se koriste za kontrolu korozije u vodoopskrbnim sustavima pitke vode, stoga postupci obrade pitke vode mogu zahtijevati praćenje fosfata i u neobrađenoj i u distribuiranoj finalnoj vodi.

Obrada otpadnih voda
Fosfor je važan hranjivi sastojak za biljke, a posebno za rast algi. Ispuštanje fosfora, zajedno s ostalim bitnim hranjivim tvarima u otpadnim vodama, potiče rast algi u potocima u koje se otpadne vode ispuštaju. Alge uzrokuju probleme s okusom i mirisom, estetski su neprivlačne i što je najvažnije, stvaraju ogromnu potrebu za kisikom kada cvat algi odumre. Iscrpljivanje kisika uzrokovano odumiranjem cvata algi otrovno je za ribe i uzrokuje druge značajne poremećaje u vodenom okruženju. Iz tih razloga regulatorne agencije često strogo reguliraju dopuštenu količinu fosfora u otpadnim vodama.
Najčešće metode uklanjanja fosfora iz otpadnih voda su biološko uklanjanje i kemijska precipitacija. Ti se postupci obično nazivaju tercijarnom obradom i zahtijevaju praćenje fosfora.

Kako se fosfor prati?

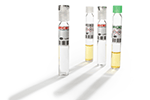
Kolorimetrijske metode (ortofosfat)
Ortofosfat (reaktivni fosfor) kombinira se s molibdatom u kiselom mediju dajući plavu ili žutu boju. Imajte na umu da nijedan analitički test nije savršen i da se s pomoću ovih testova mogu mjeriti i neki kondenzirani fosfati. Zbog kiseline se može otkriti neki suspendirani ortofosfat ako uzorak nije prvo filtriran do 0,45 mikrona. Da bi se izmjerio sav fosfor, uključujući čestice fosfata, potrebno je upotrijebiti test ukupnog fosfora koji uključuje rigoroznu razgradnju kako bi se veći dio čestica fosfata pretvorio u otopljeni oblik.
Stolni/prijenosni:
Kivetni test za fosfate (orto/ukupne) LCK349
Kivetni test za orto/ukupne fosfate LCK348
Kivetni test za fosfate (orto/ukupne) LCK350
Kivetni test za ortofosfate LCK049
Molybdovanadate TNT HR Method 8114
Reactive Phosphorus LR Chemkey (PPA)
Reactive Phosphorus HR Chemkey (PPA)
Online:

Fosfat koji se hidrolizira u kiselinu / kondenzirani fosfat
Za mjerenje kondenziranih fosfata prvo ih je potrebno pretvoriti u ortofosfat s pomoću sumporne kiseline i topline razgrađujući uzorak na 150 °C tijekom 30 minuta. To se naziva „fosfat koji se hidrolizira u kiselinu” jer se kondenzirani fosfati hidroliziraju u ortofosfat. Nakon razgradnje, za mjerenje ortofosfata koriste se metode askorbinske kiseline ili molibdovanadata. Dio organskog fosfata također će se hidrolizirati u ortofosfat, tako da rezultat nije „čisti” kondenzirani fosfat. Naravno, samim izvođenjem razgradnje i kolorimetrijskog testa dobit će se koncentracija izvornog ortofosfata i kondenziranih fosfata. Ako želite dobiti samo koncentraciju kondenziranog fosfata, jednostavno pokrenite test ortofosfata na istom uzorku bez razgradnje i oduzmite te rezultate od prve vrijednosti koncentracije.
Fosfor koji se hidrolizira u kiselinu TNT LR metoda 8180 (PhosVer 3)
Ukupni fosfor / organski fosfat
Organski fosfati su tvrdoglavi spojevi koji se ne razgrađuju lako. Da biste ih testirali, uzorak se najprije treba razgraditi s pomoću sumporne kiseline i topline, zatim treba dodati snažni oksidans poput kalijeva persulfata kako bi ortofosfati oslobodili organske veze. Nakon razgradnje, iste metode askorbinske kiseline ili molibdovanadata mogu se koristiti za mjerenje koncentracije fosfata. Opisani test pretvorit će sve različite oblike fosfata u ortofosfat, što znači da je rezultat ukupni fosfor. Ako želite znati samo koncentraciju fosfata koji je organski vezan, potrebno je provesti test hidrolize u kiselinu i oduzeti te rezultate od ukupne koncentracije fosfora (ukupne koncentracije fosfora uvijek će biti veće od koncentracije ortofosfata).
Stolni:
Kivetni test za fosfate (orto/ukupne) LCK349
Kivetni test za orto/ukupne fosfate LCK348
Kivetni test za fosfate (orto/ukupne) LCK350
Total Phosphorus TNT LR Method 8190 (PhosVer 3)
Total Phosphorus TNT HR Method 10127 (Molybdovanadate)
Mrežni:
Često postavljana pitanja
Može li se analizator Phosphax sc koristiti za ispitivanje morske vode?
Ne, Phosphax sc ne može se koristiti za ispitivanje morske vode jer ova metoda djeluje samo do 1000 mg/l klorida. Sadržaj klorida u morskoj vodi obično je veći od 19000 mg/l.
Koja je razlika između plave metode i žute metode za fosfate?
Reaktivni fosfor može se kolorimetrijski izmjeriti s pomoću nekoliko različitih kemikalija. Prvo, fosfor reagira s molibdatom u kiseloj otopini da bi stvorio kompleks fosfomolibdata. Za mjerenja niskog raspona, kompleks fosfomolibdata se reducira ili aminokiselinom ili askorbinskom kiselinom, stvarajući karakterističnu vrstu molibden plave. Mjerenja visokog raspona mogu se provesti reakcijom kompleksa fosfomolibdata s vanadijskim reagensom kako bi se dobio žuti proizvod. Intenzitet boje i plavog i žutog kompleksa proporcionalan je koncentraciji fosfora u uzorku.
DOKUMENTI I KATALOZI
UVJETI POSLOVANJA
- Pravila o dostavi i transport
- Pravila o povratu
- Hach jamstvo
- Pravila i uvjeti
- Opći uvjeti prodaje za proizvode tvrtke Hach lange d.o.o.( Europa-univerzalni]
- Sigurnost proizvoda i proces prijave kordinirane ranjivosti
- Do Not Sell or Share My Data
- Pravila o zaštiti privatnosti
- E-shop Hach
- Cookie Policy